SKB264 补充资料20240709才开始排队审评
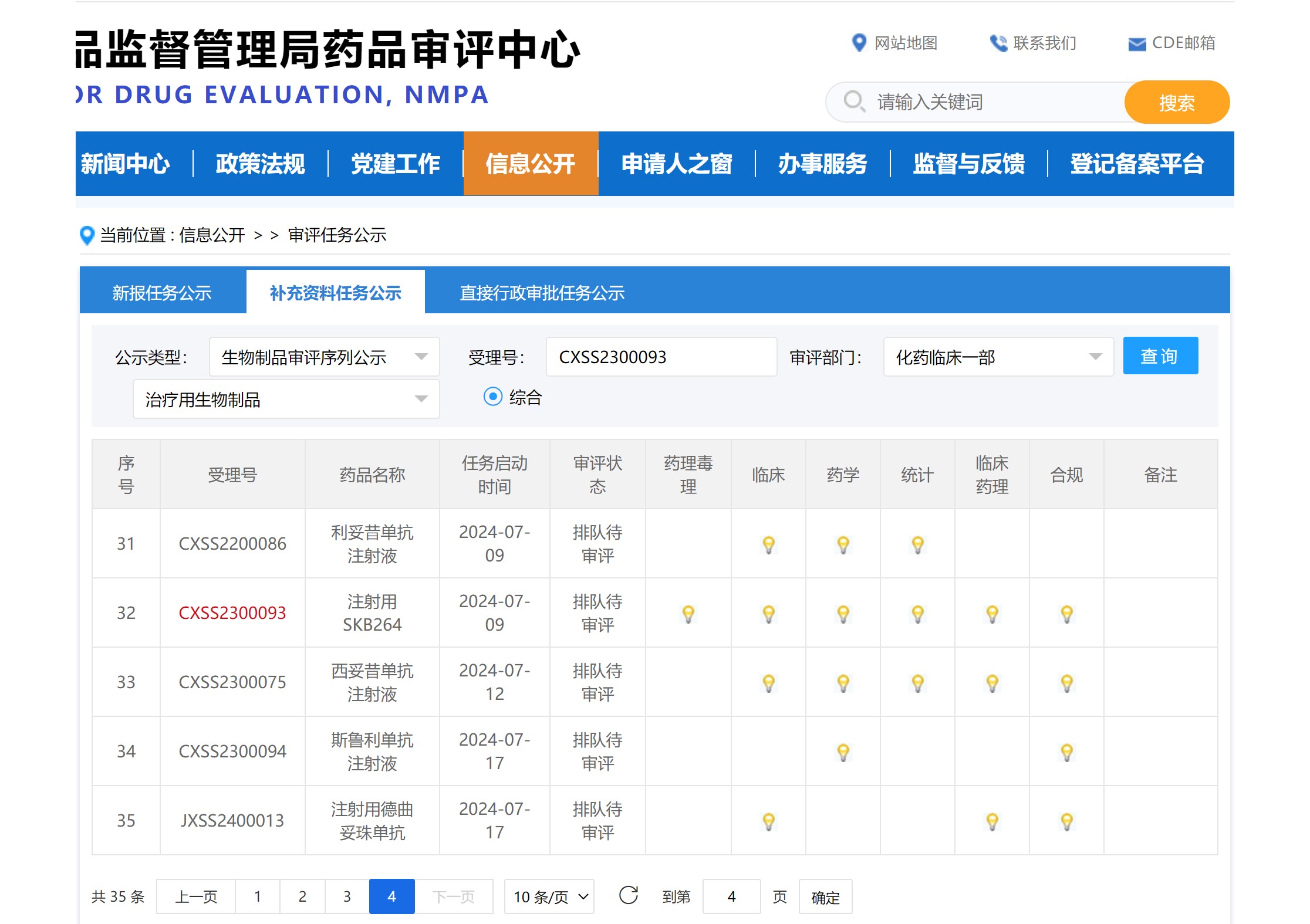
突破性疗法认定,还被纳入优先评审
2023年11月就申报了
CDE就这审评进度!
无话可说!
侯年马月才能审完?
2024-07-18 10:43:05 作者更新以下内容
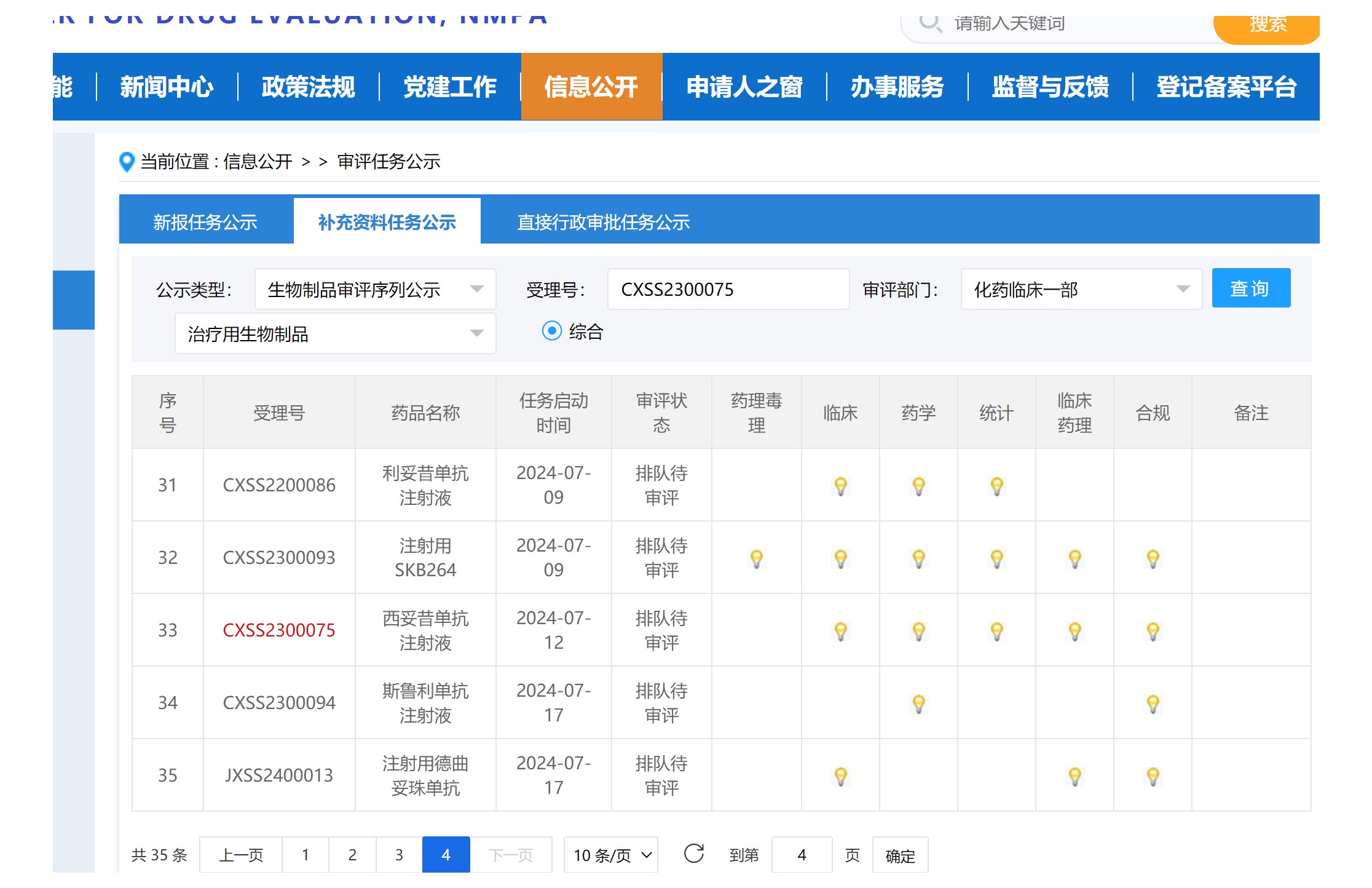
2024-07-18 10:43:48 作者更新以下内容
A140补充资料20240712才开始排队审评
2024-07-18 11:01:14 作者更新以下内容
A167 三年继续暂停排队
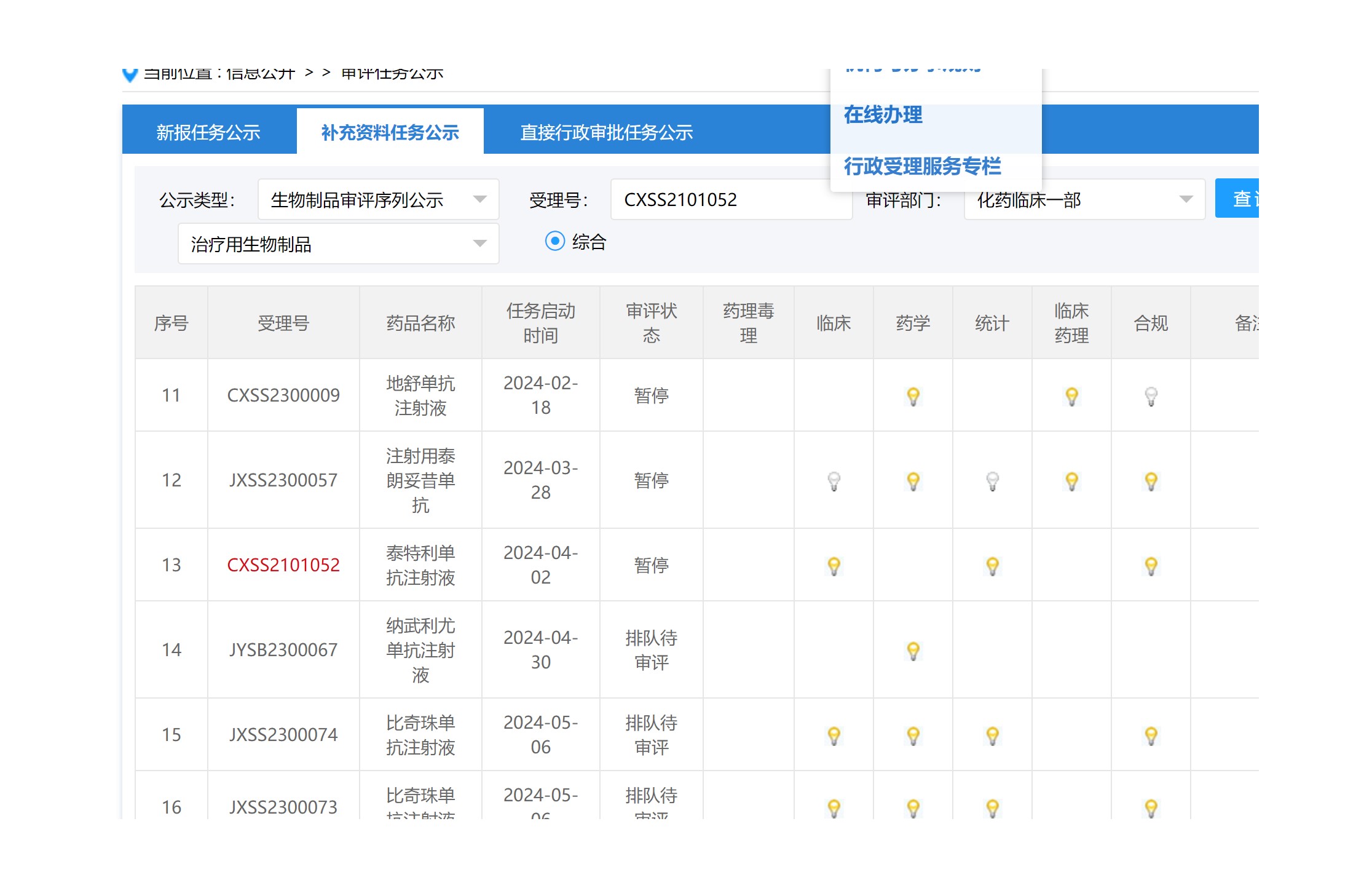
2024-07-18 11:06:06 作者更新以下内容
威武不能屈
继续审
2024-07-19 07:14:04 作者更新以下内容
从2023年12月11日算起,130个工作日刚好截止2024年6月底
现在补充资料,又要延审至哪个工作日?
2024-07-19 07:16:51 作者更新以下内容
6个专业灯亮待审到何时?
审完6个专业,还有一个综合评审要10个工作日。
2024-07-19 08:19:33 作者更新以下内容

第六条:技术评审时限要求是在130个工作日
2024-07-19 08:20:25 作者更新以下内容
第九条 第十条:综合审批审批10个工作日

2024-07-19 08:24:43 作者更新以下内容
FDA新药的审评时限主要依赖于不同的审批途径,其中优先审评是最常见的特殊认定之一。优先审评的目的是加快对具有显著治疗效果的药物的监管审评期,而不是加快药物研发过程本身。根据美国FDA的规定,优先审评应在申请受理后6个月内完成审评,而标准审批时间为10个月。这一制度旨在加快对那些能够提高有效性、消除或大幅减少限制治疗的药物反应、提高患者依从性以获得更好的疗效,或在新亚群中具有安全性和有效性的证据的药物的审评过程1。 此外,FDA通过多种手段来缩短创新药物的审评时间,包括优先审评、快速通道认定和突破性药物认定等。例如,优先审评规定FDA对新药上市申请的审评时间为6个月,而标准审评的时间为10个月2。这些措施旨在提高新药的审评效率,从而更快地将有效的药物推向市场。
2024-07-19 08:27:09 作者更新以下内容
CDE优先审批130个工作日不能保证完成,A167这类新药三年都完不成审批!为什么?
2024-07-19 15:13:55 作者更新以下内容
A140 2023年5月就申报了,都一年多了,现在又处于停顿状态!看样子,变成第二个A167 修行三年无结果!
2024-07-19 15:31:56 作者更新以下内容
漂亮国6-10个月
东大三年无果
有对比真好啊
郑重声明:用户在财富号/股吧/博客等社区发表的所有信息(包括但不限于文字、视频、音频、数据及图表)仅代表个人观点,与本网站立场无关,不对您构成任何投资建议,据此操作风险自担。请勿相信代客理财、免费荐股和炒股培训等宣传内容,远离非法证券活动。请勿添加发言用户的手机号码、公众号、微博、微信及QQ等信息,谨防上当受骗!
评论该主题
帖子不见了!怎么办?作者:您目前是匿名发表 登录 | 5秒注册 作者:,欢迎留言 退出发表新主题
郑重声明:用户在社区发表的所有资料、言论等仅代表个人观点,与本网站立场无关,不对您构成任何投资建议。用户应基于自己的独立判断,自行决定证券投资并承担相应风险。《东方财富社区管理规定》

